Содержание статьи
Эмболизация маточных артерий (ЭМА) — это современный малоинвазивный способ лечения миомы матки. С его помощью можно навсегда забыть о проблемах, которые доставляет миома: устранить симптомы заболевания, прекратить рост миоматозных узлов, восстановить и сохранить репродуктивную функцию женщины. Однако эффективность процедуры во многом зависит не только от квалификации и опыта эндоваскулярного хирурга, но и от препаратов, которые он использует.
ЭМА требует применения современного и довольно сложного одноразового инструментария. Это катетеры и микрокатетеры для введения эмболов, гидрофильные проводники, интродьюсеры, наборы для пункции артерии и, конечно, сам эмболизационный препарат — крошечные полимерные частицы, непосредственно перекрывающие кровоток в миоматозных узлах.
Когда ЭМА только начинали применять, для ее проведения использовали несферические частицы (чаще всего поливинилалкоголя) с произвольной формой. По сути, пластиковые хлопья. В последующие годы практика применения таких препаратов показала, что у них есть определенные недостатки. В настоящее время несферические частицы считаются устаревшими и не рекомендуются в качестве основного препарата для ЭМА. Однако в определенных случаях они могут применяться в комбинации с современными препаратами. Сегодня появились эмболизационные препараты, которые позволяют обеспечить высокую точность ЭМА, не вызывают воспалительной реакции и практически исключают риск возобновления кровотока в миоматозных узлах. Это так называемые сферические эмболы – частицы, имеющие правильную шарообразную форму.Теперь подробнее о характеристиках препаратов, которые применяются при эмболизации маточных артерий.
Несферические частицы PVA – самый первый эмболизационный препарат для ЭМА. Его активно использовали в первое десятилетие применения методики ЭМА – в конце 90-х и до конца 2000-х годов. К сожалению, неправильная форма частичек и связанный с этим большой разброс их линейных размеров не позволяли добиваться точной эмболизации целевых артерий миомы. Слипание частичек могло приводить к закупорке более крупной ветви, а ее более тонкая периферия оставалась свободной. Это нежелательное явление (его назвали эффектом «псевдоэмболизации») создавало риск восстановления кровоснабжения миомы в отделенном периоде. Чтобы устранить восстановление кровотока, требовалась дополнительная эмболизация.
Помимо этого, при использовании PVA возможно слипание частиц в катетере. В результате катетер нужно менять, увеличивается продолжительность вмешательства. Из-за неточных размеров частичек повышается вероятность воздействия на сосуды здоровой ткани матки.
Также частицы PVA могут вызвать выраженную воспалительную реакцию, что негативно влияет на ощущения пациентов после эмболизации.
Тем не менее, в ряде случаев PVA по-прежнему может применяться. Во-первых, «агрессивность» этого препарата и его склонность к слипанию используются для остановки кровотечений (включая послеродовые кровотечения). Во-вторых, при эмболизации сферическими частицами иногда целесообразно завершать процедуру введением небольшого количества несферического эмболизата, чтобы «запломбировать» сферы в артериях и избежать их возможного «уплотнения» под действием пульсовых волн. Это повышает эффективность ЭМА.
Развитие методики ЭМА сопровождалось бурным научно-техническим прогрессом в области эмболизационных частиц. Сейчас несферические препараты не рекомендуется применять для ЭМА по поводу миомы (кроме случаев использования в комбинации со сферами). Однако и сферические препараты прошли большой эволюционный путь. По сути, сейчас мы работаем уже с препаратами 4-го поколения. К сожалению, они недешевы и поэтому применяются далеко не везде. Во многих лечебных учреждениях до сих пор выполняют ЭМА сферами старых поколений и даже несферическим ПВА. Случается, что используют совершенно экзотические препараты, не предназначенные для ЭМА в принципе и не проходившие исследования должного формата. Такие препараты по определению не способны закрыть сосуды в миоматозных узлах

Одна из особенностей препарата Embozene заключается в высокой контрастности раствора с частицами (она значительно выше, чем у прежних аналогов). Благодаря этой особенности улучшается контроль за движением частиц во время проведения ЭМА. Это не только облегчает задачу эндоваскулярному хирургу, но и повышает эффективность процедуры.
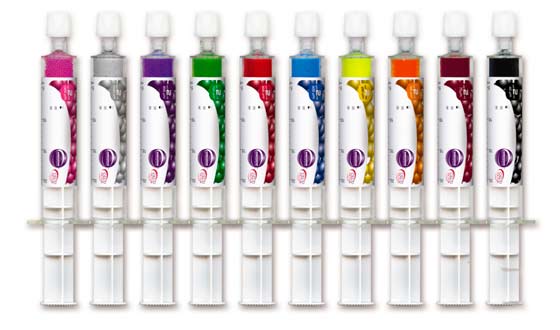
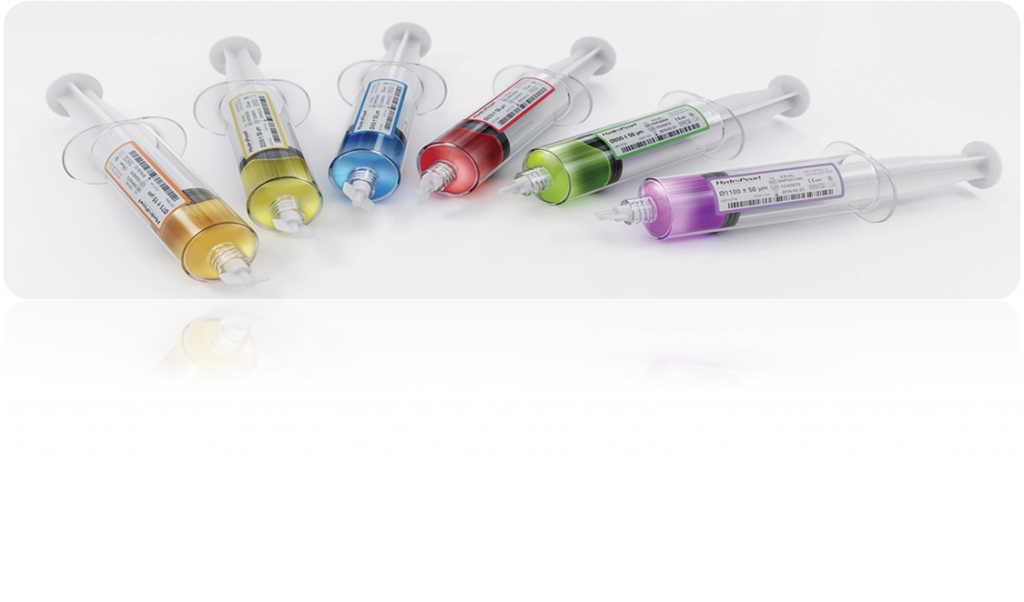
HydroPearl («Хайдропёл» или «Гидроперл») был выпущен японской компанией Terumo в 2016 году вместо снятого с производства прежнего сферического препарата Bead Block. Сейчас это самый современный эмболизационный препарат в мире. В отличие от старых аналогов, HydroPearl имеет широкую линейку размеров, микросферы в нем с высокой точностью калиброваны. Кроме того, производитель разработал принципиально новый состав препарата, обеспечивающий отличную биосовместимость микросфер.
Были проведены испытания микросфер HydroPearl на биосовместимость в соответствии с требованиями стандарта ISO 10993n. В результате исследований никаких нежелательных биологических реакций выявлено не было. Препарат после эмболизации не вызывает воспалительной реакции. Это существенно улучшает результаты ЭМА и переносимость вмешательства. Кроме того, исследования показали, что микросферы HydroPearl имеют несколько большую точность калибровки частиц, чем Embozene
Список литературы:
Ведущие специалисты
Наши услуги
Регистрация